
מחקר ופיתוח
24
http://link.springer.com/article/10.1007%2Fs10237-016-0864-4 למאמרים:
http://online.liebertpub.com/doi/abs/10.1089/ten.TEC.2016.0424 https://link.springer.com/article/10.1007/s10439-017-1814-8?wt_mc=Internal.Event.1.SEM.ArticleAuthorOnlineFirst
ג
ישה מחקרית שפותחה בטכניון תאפשר ניבוי מוקדם ומהיר של היווצרות גרורות סרטניות. מידע זה יאפשר לרופאים
לטפל בגרורות כבר בשלבים המוקדמים של התהוותן ובכך לשפר את סיכויי ההישרדות של המטופל.
ופיתוחה נמשך מאז בכמה כיוונים, המוצגים בשלושה מאמרים שפרסמה
2013-
הגישה האמורה הוצגה לראשונה ב
לאחרונה פרופ’-משנה דפנה ויס מהפקולטה להנדסה ביורפואית בטכניון. פרופ’-משנה ויס, ראש המעבדה
למכנוביולוגיה של סרטן ופצעים, חוקרת את הכוחות המכניים שמפעילים על רקמות הגוף תאים מטסטטיים - תאים
עם פוטנציאל גרורתי גבוה. המחקר נערך באמצעות משטחי ג’ל סינתטיים שיוצרו במעבדתה של פרופ’-משנה ויס
) של תאי
Metastatic Potential
ומדמים בקשיחותם רקמות רכות בגוף. המטרה: לכמת את הפוטנציאל הגרורתי (
סרטן. בניסויים במעבדה נבדקים הכוחות שמפעילים תאים כאלה על אותם משטחים כדי להידחף לתוכם.
בניגוד לטיפול בגידולים ראשוניים, הנעשה כיום ביעילות גבוהה, הטיפול בגרורות סרטניות מורכב ומאתגר. גרורות אלה
נשלחות לאיברים בריאים דרך מערכות הלימפה וכלי הדם, וקשה לזהותן בשלבי התפתחותן הראשוניים. כאשר הן
מאותרות, בדרך כלל בשלב שהן כבר גדולות ומפושטות, ההתמודדות הרפואית עמן מסובכת מאוד. זו הסיבה שגרורות
מהתמותה מסרטן.
90%-
סרטניות אחראיות לכ
בעשורים האחרונים פותחו שיטות שונות לזיהוי הפוטנציאל המטסטטי של תאים, בעיקר על סמך סמנים גנטיים
וביולוגיים. חסרונן של מדידות אלה בכך שהן יקרות, ממושכות ואינן ישימות בסוגי סרטן כגון סרטן לבלב, שעדיין לא
אופיינו בתסמינים. למעשה, עד כה לא הוצגה שיטה יעילה, מדויקת וכללית מספיק לכימות הפוטנציאל המטסטטי
החיוני לניבוי היווצרותן של גרורות.
במחקריה של פרופ’-משנה ויס נמצא כי שינויים במבנה התא ויכולתו להפעיל כוח מכני עשויים לספק את המידע
החיוני הזה בדרך כמותית מדויקת. שיטה זו, שאינה תלויה בגנטיקה הספציפית של הגידול, מאפשרת מדידה מהירה
(בשעות ספורות) ומותאמת אישית לחולה.
משטחי הג’ל הסינתטיים שפיתחה פרופ’-משנה ויס דומים ברמת הקושי שלהם לרקמות רכות וכך מאפשרים לחקור
את התנאים שבהם מפעילים התאים כוח על הרקמה שלתוכה הם מנסים לחדור. שיטה זו מאפשרת לכמת את
מידת הכוח שהם מפעילים ואת ההבדל בהתנהגותם של סוגי תאים שונים. “מעניין לציין שבתנאים מסוימים הסוד
- התא הסרטני רך וגמיש יותר מתא בריא, והתא המטסטטי רך
רכּוּת
אלא דווקא
קשיוּת
של התאים הסרטניים אינו
וגמיש אף יותר. התאים הסרטניים מסתגלים לסביבה במהירות, והשיטה שלנו מבוססת על זיהוי השינויים שחלים בהם
ומאפשרים להם להיות רכים או להתקשח ולהפעיל כוח כדי שיוכלו להתנייד בסביבות שונות. עם התגליות החדשות
אנחנו מתכוונים ללכת הלאה ולפתח ניבוי מהיר וכמותי של היווצרות גרורות על סמך אותה תנועה קבוצתית של תאים.”
לאחרונה החלה פרופ’-משנה ויס בבדיקת השיטה על גידולים שהוצאו מגופם של חולי סרטן הלבלב, הקיבה והשד ועל
גידולים מסוג סרקומה ע”ש יואינג האופיינית לילדים ולנוער. המחקר נעשה באישור ועדת הלסינקי.
פרופ’-משנה ויס מציינת שהתוצאות הראשוניות מעודדות ומבהירה שהמחקר מבוסס על “שאריות” של רקמות גידול
שאין בהן שום צורך, אפילו מבחינת הבדיקה הפתולוגית.
גורלית
התרעה
בפקולטה להנדסה ביו-רפואית פותחה שיטה חדשה לאומדן הפוטנציאל הגרורתי של גידולים סרטניים
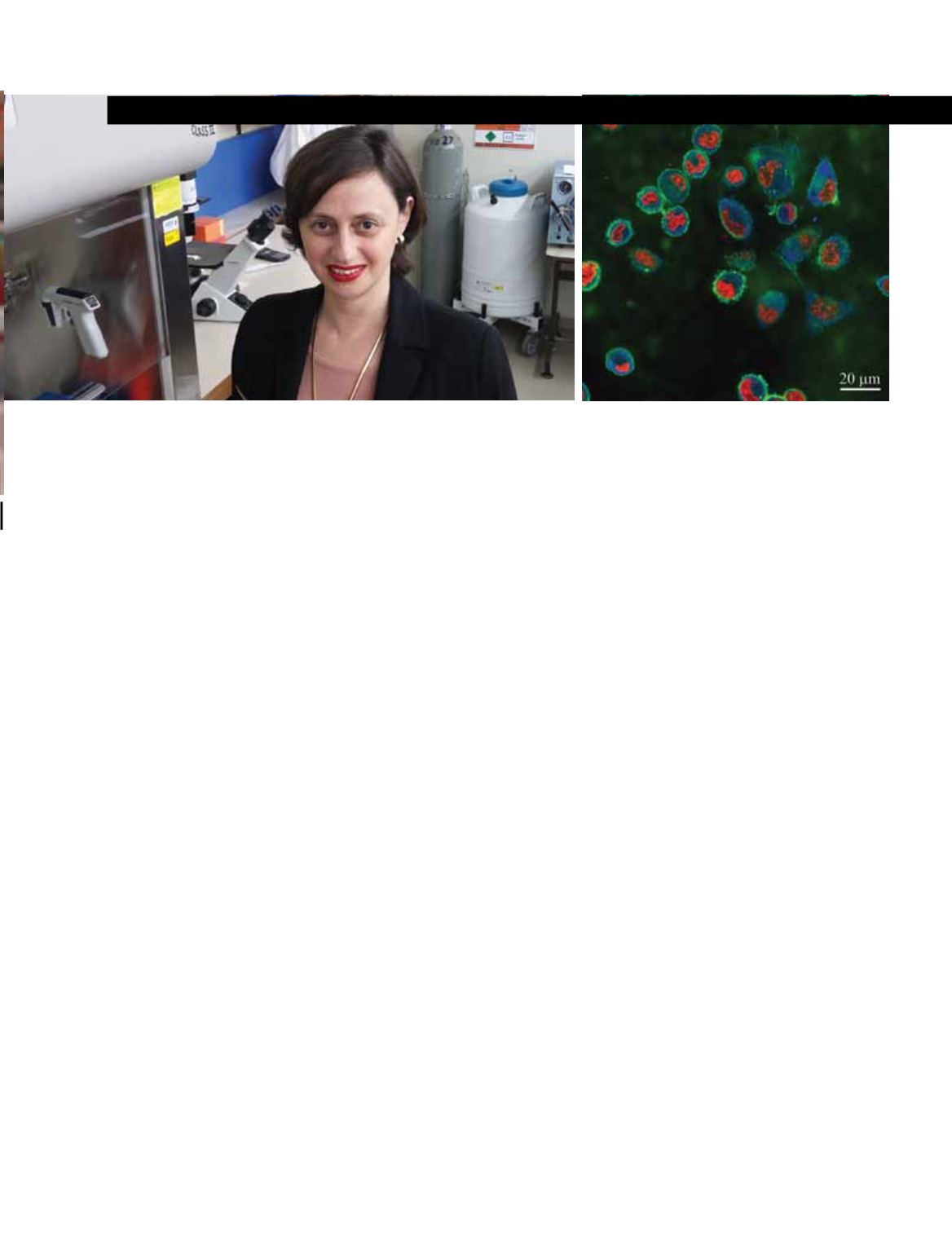
תמונת חתך ממיקרוסקופ
קונפוקלי: תאי סרטן
שד בעלי פוטנציאל
מטסטטי גבוה נדחפים
לתוך ג’ל פוליאקרילאמיד
בקשיחות. בתמונה אפשר
לראות את גרעיני התאים
(אדום),
את אלמנט האקטין
בשלד התוך תאי (ירוק)
ואת חיבורי התאים
למשטח במוקדי חיבור
(כחול)
פרופ’-משנה דפנה ויס
















